 й«ҳзә§дјҡе‘ҳ
й«ҳзә§дјҡе‘ҳ
 е·Іи®ӨиҜ?/p>
е·Іи®ӨиҜ?/p>
Langmuir

1916 е№ҙпјҢI. Langmuir жҸҗеҮәеҚ•еұӮеҗёйҷ„зҗҶи®ә[1]пјҢеҹәдәҺдёҖдәӣжҳҺзЎ®зҡ„еҒҮи®ҫжқЎд»¶пјҢеҫ—еҲ°з®ҖжҳҺзҡ„еҗёйҷ„зӯүжё©ејҸвҖ Langmuir ж–№зЁӢгҖӮиҜҘејҸйҮҮз”ЁзғӯеҠӣеӯҰгҖҒз»ҹи®ЎеҠӣеӯҰе’ҢеҠЁеҠӣеӯҰж–№жі•еқҮеҸҜеҜјеҮәгҖӮLangmuir еҗёйҷ„зӯүжё©ејҸж—ўеҸҜеә”з”ЁдәҺеҢ–еӯҰеҗёйҷ„пјҢд№ҹеҸҜд»Ҙз”ЁдәҺзү©зҗҶеҗёйҷ„пјҢеӣ иҖҢеңЁеӨҡзӣёеӮ¬еҢ–з ”з©¶дёӯеҫ—еҲ°жңҖжҷ®йҒҚзҡ„еә”з”ЁгҖҒь/span>
еҚ•еҲҶеӯҗеұӮеҗёйҷ„зӯүжё©ејҺь/strong>
Langmuir жЁЎеһӢзҡ„еҹәжң¬еҒҮи®ҫдёәпјҷьbr style="margin: 0px; padding: 0px; outline: 0px; max-width: 100%; box-sizing: border-box; overflow-wrap: break-word !important;"/>
в‘ еҗёйҷ„еүӮиЎЁйқўеӯҳеңЁеҗёйҷ„дҪҚпјҢеҗёйҷ„иҙЁеҲҶеӯҗеҸӘиғҪеҚ•еұӮеҗёйҷ„дәҺеҗёйҷ„дҪҚдёҠпјӣ
в‘ еҗёйҷ„дҪҚеңЁзғӯеҠӣеӯҰе’ҢеҠЁеҠӣеӯҰж„Ҹд№үдёҠжҳҜеқҮдёҖзҡ„пјҲеҗёйҷ„еүӮиЎЁйқўжҖ§иҙЁеқҮеҢҖпјүпјҢеҗёйҷ„зғӯдёҺиЎЁйқўиҰҶзӣ–еәҰж— е…іпјӣ
в‘ еҗёйҷ„еҲҶеӯҗй—ҙж— зӣёдә’дҪңз”ЁпјҢжІЎжңүжЁӘеҗ‘зӣёдә’дҪңз”Ёпјӣ
в‘ еҗёйҷ„вҖ”и„ұйҷ„иҝҮзЁӢеӨ„дәҺеҠЁеҠӣеӯҰе№іиЎЎд№ӢдёӯгҖҒь/span>
Оё=V/Vm=ap /(1+ ap) (1)[2,3]
ејҸдёӯпјҢО дёәиЎЁйқўиҰҶзӣ–еәҰпјҢV дёәеҗёйҷ„йҮҸпјҢVm иЎЁзӨәеҚ•еұӮеҗёйҷ„е®№йҮҸпјҢp жҳҜеҗёйҷ„иҙЁи’ёжұҪеҗёйҷ„е№іиЎЎж—¶зҡ„еҺӢеҠӣпјҢaдёәеҗёйҷ„зі»ж•°пјҢжҳҜеҗёйҷ„е№іиЎЎеёёж•°гҖҒь/span>
еӣ? дёәејҸ1 жҸҸиҝ°зҡ Langmuir еһӢеҗёйҷ„зӯүжё©зәҝпјҢеұһдәҺIUPAC еҲҶзұ»зҡ„I еһӢзӯүжё©зәҝгҖӮеңЁеҺӢеҠӣеҫҲдҪҺжҲ–иҖ…еҗёйҷ„еҫҲејұж—¶пјҢО = apпјҢеҗёйҷ„йҮҸдёҺе№іиЎЎеҺӢеҠӣжҲҗжӯЈжҜ”пјҲHenry е®ҡеҫӢпјүпјӣеңЁеҺӢеҠӣеҫҲеӨ§жҲ–иҖ…еҗёйҷ„еҫҲејәж—¶пјҢО вү 1пјҢеҗёйҷ„йҮҸдёәеҚ•еұӮеҗёйҷ„е®№йҮҸпјҢдёҺеҺӢеҠӣж— е…ігҖҒь/span>
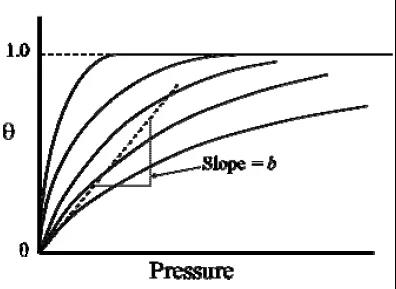
еӣ? Langmuir еһӢеҗёйҷ„зӯүжё©зәҝ
Langmuirе…¬ејҸдҪҝз”Ё
иҷҪ然Langmuir е…¬ејҸжҳҜдёҖдёӘзҗҶжғізҡ„еҗёйҷ„е…¬ејҸпјҢд»ЈиЎЁдәҶеңЁеқҮеҢҖиЎЁйқўпјҢеҗёйҷ„еҲҶеӯҗеҪјжӯӨжІЎжңүдҪңз”ЁпјҢиҖҢдё”еҗёйҷ„жҳҜеҚ•еҲҶеӯҗеұӮжғ…еҶөдёӢеҗёйҷ„иҫҫеҲ°е№іиЎЎж—¶зҡ„规еҫӢпјҢдҪҶжҳҜеңЁе®һи·өдёӯдёҚд№ҸдёҺе…¶зӣёз¬Ұзҡ„е®һйӘҢз»“жһңгҖӮиҝҷеҸҜиғҪжҳҜе®һйҷ…йқһзҗҶжғізҡ„еӨҡз§Қеӣ зҙ дә’зӣёжҠөж¶ҲжүҖиҮҙгҖӮдҫӢеҰӮеҗёйҷ„иҙЁеҲҶеӯҗй—ҙзҡ„зӣёдә’дҪңз”ЁдёҖиҲ¬йҡҸиҰҶзӣ–еәҰзҡ„жҸҗй«ҳиҖҢеҠ ејәпјӣиҖҢеҗҢж—¶еңЁдёҚеқҮеҢҖзҡ„иЎЁйқўпјҢеҗёйҷ„йҰ–е…ҲеҸ‘з”ҹеңЁй«ҳиғҪзҡ„еҗёйҷ„дҪҚдёҠпјҢеҗёйҷ„зғӯйҡҸиҰҶзӣ–еәҰеўһеҠ иҖҢдёӢйҷҚгҖӮиҝҷдёӨз§Қеӣ зҙ зӣёдә’жҠөж¶ҲпјҢеңЁдёӯзӯүзҡ„иҰҶзӣ–еәҰиҢғеӣҙ Оё = 0.1~0.4пјҢa еҖјиҝ‘дјјдёәеёёж•°гҖӮеӣ иҖҢеңЁжӯӨиҢғеӣҙеҶ…еҗёйҷ„зӯүжё©зәҝеҸҜз” Langmuir е…¬ејҸиЎЁеҫҒгҖҒь/span>
йңҖиҰҒжҢҮеҮәзҡ„жҳҜпјҢеҜ№дәҺзү©зҗҶеҗёйҷ„ Langmuir е…¬ејҸеҸҜд»ҘжҸҸиҝ° I еһӢзӯүжё©зәҝпјҢдҪҶжҳ I еһӢзӯүжё©зәҝеҫҖеҫҖеҸҚжҳ зҡ„жҳҜеҫ®еӯ”еҗёйҷ„еүӮзҡ„еҫ®еӯ”еЎ«е……зҺ°иұЎпјҢжһҒйҷҗеҗёйҷ„йҮҸжҳҜеҫ®еӯ”зҡ„еЎ«е……йҮҸгҖӮеңЁдёӯзӯүзҡ„зӣёеҜ№еҺӢеҠӣеҗҺпјҢеӣәдҪ“иЎЁйқўзҡ„еҗёйҷ„йҮҸйғҪжңүжҳҺжҳҫзҡ„еўһеӨ§пјҢиЎЁжҳҺеҸ‘з”ҹеӨҡеұӮеҗёйҷ„гҖӮиҝҷе°ұжҳҜ BET еӨҡеұӮеҗёйҷ„жЁЎеһӢзҡ„з”ұжқҘгҖҒь/span>
еҸӮиҖғж–ҮзҢ?/span>
[1]Langmuir I. The Constitution and Fundamental Properties of Solids and Liquids. Part I. Solids. J. Am. Chem. Soc., 1916, 38(11):2221
[2] Dabrowski A. Adsorption - from theory to practice. Adv. Colloid Interface Sci., 2001, 93:135
[3] Langmuir I. The Adsorption of Gases on Plane Surfaces of Glass, Mica and Platinum. J. Am. Chem. Soc., 1918,40(9):1361
- е…ЁиҮӘеҠЁжҜ”иЎЁйқўз§ҜдёҺеӯ”еҫ„еҲҶжһҗд»?/a>
- е…ЁиҮӘеҠЁеҢ–еӯҰеҗёйҷ„д»Ә
- е…ЁиҮӘеҠЁз”өжўҜеҚҮйҷҚе…«з«ҷи„ұж°”з«ҷGM7842
- еҸҢз«ҷжҢҜе®һеҜҶеәҰд»ӘTM5120зі»еҲ—
- е…ЁиҮӘеҠЁеӣӣз«ҷзңҹеҜҶеәҰд»ӘDM6140зі»еҲ—
- е…ЁиҮӘеҠЁеҸҢз«ҷеҢ–еӯҰеҗёйҷ„д»ӘCM8320
- е…ЁиҮӘеҠЁеҚ•з«ҷеҢ–еӯҰеҗёйҷ„д»ӘCM8310
- е…ЁиҮӘеҠЁй«ҳеҺӢеҗёйҷ„д»ӘHP6500зі»еҲ—
- е…ЁиҮӘеҠЁеҫ®еӯ”зү©зҗҶеҗёйҷ„д»ӘPM7200


