 白金会员
白金会员
 已认�?/p>
已认�?/p>
本文摘要
在肿瘤治疗中展现强大治疗潜力皃�/span>ADC药物,其大规模商业化很大程度上是基于偶联技术的突破,更智能的连接子真正实现药物的精准释放,�?/span>ADC药物的疗效和安全性得到了显著的提升。为应对ADC药物极高的研发成本,降低失败风险,表征关键质量属性(CQAs)是此类药物研发生产的关键所在。本文介绍了马尔文帕纳科贯穿ADC药物研发全过程的多种表征技术及其在评估结合活性、优化稳定性及控制颗粒形成等领域的相关应用、�/span>
近年来,抗体偶联药物'�/span>Antibody-Drug Conjugates, ADCs)逐渐成为生物技术领域的明星产品,其独特的机刵�/span>—–�span style="font-family:等线">结合抗体的靶向性与高毒性小分子药物的强效杀伤力,为癌症治疗提供了精准且高效的解决方案。根据最新数据,全球癌症患者每年新增约2000万例,耋�/span>ADC药物已在肿瘤治疗中展现出强大的治疗潜力。以Enhertu为例+�/span>2023年该药物为其开发者阿斯利康(AstraZeneca)和第一三共'�/span>Daiichi Sankyo)带来了25亿美元的销售收入,成为多个ADC‛�span style="font-family:等线">重磅炸弹“�span style="font-family:等线">药物之一、�/span>2023年,全球ADC市场总规模首次突破百亿美元大关、�/span>在中国市场,ADC领域同样发展迅猛+�/span>2024年多欽�/span>ADC产品通过License-out模式实现了高额交易,为行业注入了强劲的增长动力、�/span>
ADC药物的崛起并非偶然,其成功得益于多年来生物技术的进步和创新。单克隆抗体的研发已经有运�/span>40年的历史+�/span>ADC所使用的高毒性药物(妁�/span>DNA和微管抑制剂)也有着长期的研究基础。但真正推动ADC大规模商业化的是近年来偶联技术的突破、�/span>
早期的连接子'�/span>linker)技术因化学稳定性差而导致药物在非特定位置释放,显著缩小了治疗窗口。此外,连接子的容量有限,也限制了抗体所能携带药物的数量。而过厺�/span>10-15年中,随着更智能的连接子被设计出来,通过pH敏感性或靶细胞内切割机制实现药物的精准释放,ADC的疗效和安全性得到了显著提升。这些技术进步极大地扩展亅�/span>ADC的治疗窗口,降低了药物对健康组织的副作用,同时最大化了对病变组织的打击力度、�/span>
ADC药物的研发成本极高,同时面临着失败风险。表征关键质量属性(CQAs)是降低研发风险、提高产品成功率的关键所在、�/span>
01�?strong>关键质量属性表征的挑战与机遆�/strong>
ADC药物的成功依赖于多个因素,包括抗体与抗原结合后的效果、药物载荷对抗体稳定性的影响,以及聚集行为等。其中,以下问题尤为关键9�/span>
偶联对结合活性的影响9�/span>常用的赖氨酸偶联策略可能改变抗体的结合区域,从而降低药物靶向性与疗效、�/span>
抗体稳定性的降低9�/span>偶联的高疏水性小分子药物往往会影响抗体的结构稳定性,增加聚集倾向,缩短药物保质期、�/span>
亚微米颗粒的形成9�/span>亚微米颗粒可能引发免疫原性反应,是监管机构日益关注的重点、�/span>
面对ADC研发中的复杂挑战,马尔文帕纳科提供了一系列先进的表征工具,覆盖研发全过程,帮助企业科学应对问题并优化开发效率、�/span>
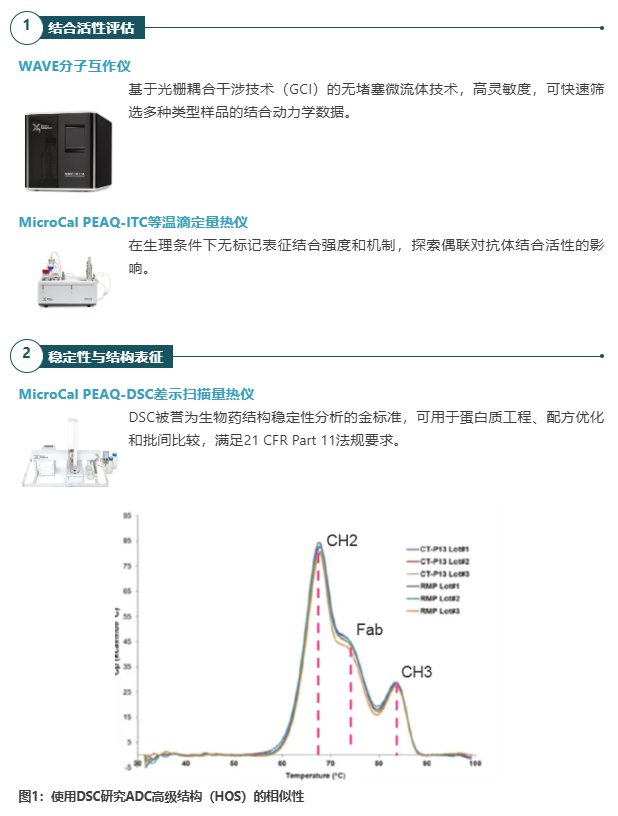
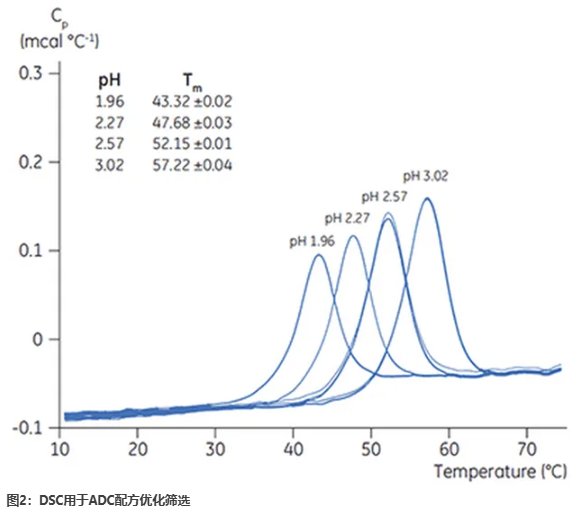

从研发到生产的全程支�?/span>
马尔文帕纳科的技术与专业知识贯穿ADC药物的研发全过程,无论是评估结合部位与活性、优化稳定性,还是控制颗粒形成,都能为企业提供全面支持。在这个充满潜力的领域,我们助力研发企业在提高效率和质量的同时,降低研发失败的风险,帮助更多创新疗法造福患者、�/span>


